Amiloidosi da transtiretina: iter diagnostico e approccio...
Nell’amiloidosi cardiaca il sospetto clinico è la chiave di...
Alberto è un uomo di 68 anni che presenta numerosi fattori di rischio cardiovascolare: è affetto da cardiopatia ipertensiva, con un buon controllo della pressione a domicilio con terapia specifica che assume regolarmente. Conduce una vita attiva partecipando a corse amatoriali in bicicletta. Esegue da anni visite cardiologiche con elettrocardiogramma (ECG) ed ecocardiogramma per poter proseguire l'attività sportiva.
Da un anno lamenta un progressivo peggioramento della tolleranza allo sforzo per dispnea per sforzi moderati (classe NYHA II) che attribuisce all’età e al decondizionamento fisico dopo il periodo del lockdown, durante il quale è anche aumentato di peso.
Accede in Pronto Soccorso del nostro ospedale per dolore toracico e qui, nel sospetto di sindrome coronarica acuta, vengono eseguiti un ECG ed il dosaggio seriato della troponina sierica ad alta sensibilità.
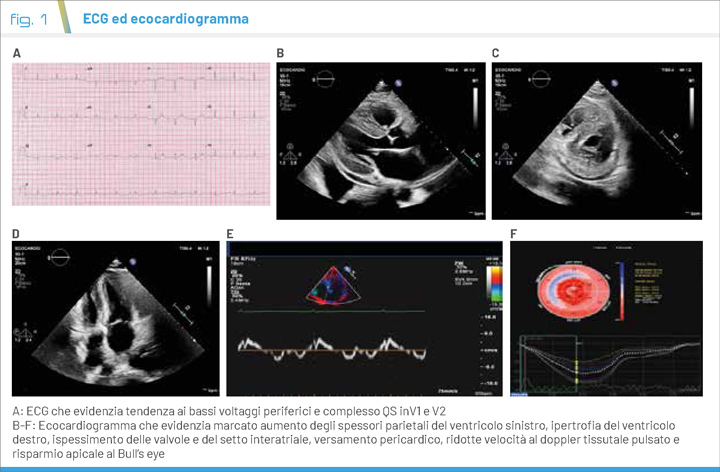
L’ECG (Fig. 1A) mostra bassi voltaggi nelle derivazioni periferiche (specialmente se confrontati al quadro ecocardiografico di nota ipertrofia ventricolare sinistra) e delle onde Q (segno di pregressa necrosi) in V1 e V2, ma non sono presenti alterazioni acute della ripolarizzazione suggestive di ischemia. Il dosaggio della troponina mostra elevati valori pur in assenza di variazioni significative a distanza di 1 e 3 ore (troponina I ultrasensibile: 68 – 72- 74 ng/l con valore normale < 4 ng/l ), l’NTproBNP (frammento amino terminale del peptide natriuretico cerebrale) è pari a 1010 pg/ml (valore normale < 450 pg/ml).
L’ecocardiogramma (Fig. 1 B-F) mostra un ventricolo sinistro di normali dimensioni con funzione sistolica globale e segmentaria conservata (frazione di eiezione: 62%) e spessori parietali marcatamente aumentati in modo concentrico. Sono evidenti anche: a) un’ipertrofia del ventricolo destro; b) un ispessimento delle valvole con insufficienza mitralica lieve; c) un versamento pericardico minimo; d) una disfunzione diastolica. A fronte di una funzione sistolica preservata le velocità al doppler tissutale pulsato sono ridotte (Onda S settale 5 cm/s) e il global longitudinal strain (GLS ) risulta ai limiti inferiori (-17%) con un risparmio dei segmenti apicali (apical sparing).
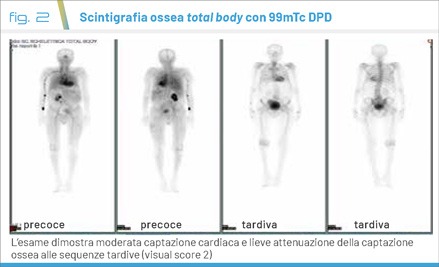 A questo punto viene sospettata un’amiloidosi cardiaca e viene eseguita una scintigrafia ossea total-body con difosfonato (DPD) che mostra una moderata captazione cardiaca con riduzione della captazione ossea (Bologna score 2) (Fig. 2). Gli esami di laboratorio per la ricerca di una componente monoclonale mostrano una positività dell’immunofissazione sierica per IgA kappa, con dosaggio delle catene libere kappa aumentate: 52,6 mg/l e un rapporto kappa/lambda alterato: 1,8.
A questo punto viene sospettata un’amiloidosi cardiaca e viene eseguita una scintigrafia ossea total-body con difosfonato (DPD) che mostra una moderata captazione cardiaca con riduzione della captazione ossea (Bologna score 2) (Fig. 2). Gli esami di laboratorio per la ricerca di una componente monoclonale mostrano una positività dell’immunofissazione sierica per IgA kappa, con dosaggio delle catene libere kappa aumentate: 52,6 mg/l e un rapporto kappa/lambda alterato: 1,8.
Viene spiegata al paziente l’importanza di raggiungere una diagnosi eziologica precisa specialmente alla luce delle possibilità terapeutiche oggi disponibili e Alberto accetta di sottoporsi ad una biopsia endomiocardica (un esame eseguito in regime di Day Hospital tramite accesso giugulare in anestesia locale). La biopsia conferma la presenza di depositi di amiloide, ma l’analisi immunoistochimica non risulta dirimente, mostrando una reattività diffusa sia per la transtiretina che per le catene kappa e lambda. Solo la spettrometria di massa permetterà di raggiungere la diagnosi definitiva di amiloidosi da transtiretina.
Il paziente viene, infine, sottoposto ad analisi genetica che risulta positiva per la mutazione Ile68Leu, tipica nella regione dell’appennino Tosco-Emiliano. Sulla base dell’analisi genetica, viene posta una diagnosi definitiva di amiloidosi cardiaca da transtiretina, secondaria a mutazione Ile68Leu, con associata gammopatia monoclonale. La valutazione del quadro neurologico è risultata negativa e Alberto ha iniziato terapia specifica con tafamidis 61 mg.
Discussione
L’amiloidosi cardiaca è una patologia causata dalla deposizione progressiva di diverse proteine nell’interstizio di diversi organi e tessuti.
Le forme che più frequentemente interessano il cuore sono quella da catene leggere delle immunoglobuline e quella da transtiretina sia nella sua forma mutata che in quella wild-type (1). È una patologia rara e poco conosciuta, sottodiagnosticata per l’aspecificità dei sintomi iniziali (2-3). Questo caso evidenzia alcuni aspetti importanti:
- è necessario “porre il sospetto” per poter giungere ad una diagnosi corretta: il paziente era seguito in ambiente cardiologico da anni, ma il suo quadro ecocardiografico era stato “etichettato” come cardiopatia ipertensiva e mai ridiscusso (4)
- grazie all’algoritmo di Gillmore è possibile raggiungere una diagnosi di certezza in un'ampia quota di pazienti mediante una scintigrafia ossea total-body ed i corretti esami di laboratorio (immunofissazione sierica, immunofissazione urinaria, dosaggio delle catene leggere libere kappa e lambda) (5-6)
- nei casi in cui l’applicazione dell’algoritmo diagnostico non invasivo non porti ad una diagnosi di certezza, è necessario “andare a fondo” con esami di secondo livello (in questo caso una biopsia endomiocardica) che permettano di raggiungere una corretta diagnosi eziologica, dal momento che la forma di amiloidosi da transtiretina e quella da catene leggere hanno prognosi e trattamenti molto differenti (7)
- ad oggi l’amiloidosi da transtiretina non è più una patologia incurabile, per cui il raggiungimento di una corretta diagnosi ha delle implicazioni terapeutiche importanti (8-9)
- l’amiloidosi è una malattia sistemica e la collaborazione di diversi specialisti (in questo caso cardiologo, ematologo, anatomopatologo e neurologo) è fondamentale nella gestione del paziente.
Conclusioni
Nell’amiloidosi cardiaca, così come in altre patologie, il sospetto clinico è la chiave di volta per la corretta cura del paziente. La prevalenza di amiloidosi cardiaca tra i pazienti con ipertrofia ventricolare sinistra e funzione sistolica preservata non è trascurabile e numerose Red Flags possono aiutarci nel sospettare questa patologia ed avviare il corretto iter diagnostico. La disponibilità di diverse linee di trattamento obbliga il clinico al raggiungimento di una corretta diagnosi di certezza per le importanti implicazioni prognostiche che ne derivano.
Nei pazienti con gammapatia monoclonale è inoltre necessario proseguire il monitoraggio laboratoristico (immunofissazione sierica, urinaria, dosaggio delle catene leggere libere kappa e lambda e proteinuria delle 24 ore) per intercettare un eventuale sviluppo di amiloidosi da catene leggere in sovrapposizione alla malattia da transtiretina.
Bibliografia
- Garcia-Pavia P, Rapezzi C, Adler Y, et al. Diagnosis and treatment of cardiac amyloidosis: a position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2021;42(16):1554-1568.
- Merlo M, Pagura L, Porcari A, et al. Unmasking the prevalence of amyloid cardiomyopathy in the real world: results from Phase 2 of the AC-TIVE study, an Italian nationwide survey. Eur J Heart Fail. 2022;24(8):1377-1386.
- Rapezzi C, Quarta CC, Obici L, et al. Disease profile and differential diagnosis of hereditary transthyretin-related amyloidosis with exclusively cardiac phenotype: an Italian perspective. Eur Heart J. 2013;34(7):520-8.
- Rapezzi C, Arbustini E, Caforio AL, et al. Diagnostic work-up in cardiomyopathies: bridging the gap between clinical phenotypes and final diagnosis. A position statement from the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2013;34(19):1448-58.
- Perugini E, Guidalotti PL, Salvi F, et al. Noninvasive etiologic diagnosis of cardiac amyloidosis using 99mTc-3,3-diphosphono-1,2-propanodicarboxylic acid scintigraphy. J Am Coll Cardiol. 2005;46(6):1076-84.
- Gillmore JD, Maurer MS, Falk RH, et al. Nonbiopsy Diagnosis of Cardiac Transthyretin Amyloidosis. Circulation. 2016;133(24):2404-12.
- Maleszewski JJ. Cardiac amyloidosis: pathology, nomenclature, and typing. Cardiovasc Pathol 2015;24:343–350.
- Grogan M, Scott CG, Kyle RA, et al. Natural History of Wild-Type Transthyretin Cardiac Amyloidosis and Risk Stratification Using a Novel Staging System. J Am Coll Cardiol. 2016 Sep 6;68(10):1014-20. doi: 10.1016/j.jacc.2016.06.033. Erratum in: J Am Coll Cardiol. 2017 Jun 13;69(23):2882. PMID: 27585505.
- Emdin M, Aimo A, Rapezzi C, et al. Treatment of cardiac transthyretin amyloidosis: an update. Eur Heart J. 2019;40(45):3699-3706.





