Calcolosi renale secondaria a cistinuria: racconto di un percorso...
La calcolosi renale è l’unica manifestazione clinica della...
Prevalenza e manifestazione clinica
La calcolosi renale secondaria a cistinuria rappresenta una causa rara di calcolosi renale, con una prevalenza dell’1-2% nella popolazione adulta che sale al 6-8% nella popolazione pediatrica (1).
La calcolosi renale è l’unica manifestazione clinica della cistinuria (OMIM 220100), malattia ereditaria autosomica recessiva caratterizzata da un difetto di trasporto a livello del tubulo renale prossimale che non è in grado di riassorbire l’aminoacido cistina e gli altri dibasico aminoacidi (ornitina, lisina, arginina – acronimo C.O.L.A.).
Solo la cistina è insolubile nelle urine al pH fisiologico e precipita nelle vie urinarie formando i calcoli. La diagnosi solitamente viene formulata quando la cistina si riscontra come componente unico o predominante in un calcolo o nel caso di familiarità. La cistinuria colpisce globalmente circa 1/7000 nuovi nati, con ampie differenze demografiche, 1/2500 negli ebrei libici e 1/100.000 in Svezia; la prevalenza stimata in Europa e USA è di circa 1/10.000 individui (2-3).
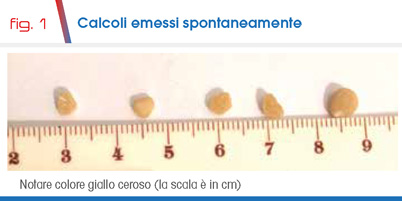 Giunge alla nostra attenzione Luca per una calcolosi recidivante calcica molto attiva in monorene congenito pelvico con severa morbilità urologica. In una occasione esame chimico di frammenti emessi: calcio ossalato. I primi esami metabolici non hanno documentato evidenti fattori di rischio per la calcolosi. Abbiamo inviato vari calcoli nel frattempo emessi (Fig. 1) per analisi cristallografica con esito di composizione di CISTINA PURA e dosaggio gascromatografico dei dibasico aminoacidi urinari risultati elevati, indicativi di stato omozigote per cistinuria (cistina 478 mg/g creatinina, valori diagnostici > 300) (4).
Giunge alla nostra attenzione Luca per una calcolosi recidivante calcica molto attiva in monorene congenito pelvico con severa morbilità urologica. In una occasione esame chimico di frammenti emessi: calcio ossalato. I primi esami metabolici non hanno documentato evidenti fattori di rischio per la calcolosi. Abbiamo inviato vari calcoli nel frattempo emessi (Fig. 1) per analisi cristallografica con esito di composizione di CISTINA PURA e dosaggio gascromatografico dei dibasico aminoacidi urinari risultati elevati, indicativi di stato omozigote per cistinuria (cistina 478 mg/g creatinina, valori diagnostici > 300) (4).
Primo ostacolo nel percorso diagnostico: diagnosi fallace di calcolosi calcica per verosimile errore nell’esame chimico dei calcoli.
I cistinurici possono formare anche calcoli misti, con altri componenti come il calcio ossalato, l’acido urico o la struvite, ma la cistina deve essere la componente predominante. L’esame chimico non è attualmente consigliabile, mentre si preferisce per una maggiore accuratezza diagnostica la spettrofotometria all’IR o l’indagine cristallografica. Una diagnosi corretta è fondamentale in quanto la terapia specifica per la calcolosi di cistina differisce sostanzialmente da quella per la calcolosi calcica. Inoltre la calcolosi cistinica, se non diagnosticata e trattata, può causare insufficienza renale fino al 70% dei soggetti (5).
 Viene formulata diagnosi di cistinuria, malattia rara del gruppo dei Disturbi del Metabolismo e del Trasporto degli Aminoacidi, codice di esenzione RCG040 (Tab. 1).
Viene formulata diagnosi di cistinuria, malattia rara del gruppo dei Disturbi del Metabolismo e del Trasporto degli Aminoacidi, codice di esenzione RCG040 (Tab. 1).
Anche se non utile a scopo diagnostico, è stato effettuato lo studio molecolare dei geni associati a cistinuria che ha identificato la presenza della duplicazione E5_E9dup in omozigosi del gene SLC3A1, nota in letteratura come associata alla cistinuria di tipo A (4).
Il trattamento della cistinuria ha come scopo la prevenzione delle recidive calcolotiche, mantenendo le urine sottosature per la cistina, al di sotto del limite di solubilità che è di 250 mg/L, ma che aumenta a 500 mg/L ad un pH di 7,5 (6). Luca ha una cistinuria di circa 1000 mg/24 ore, per cui deve garantire una diuresi alcalina di circa 3-4 L con iperidratazione frazionata durante la giornata, prima del riposo notturno ed eventualmente nei risvegli notturni. Per alcalinizzare le urine, è consigliabile un citrato di potassio a formulazione retard con possibilità di monitorare le dosi secondo il pH delle urine con cartine tornasole, in compresse da assumere 2-3 volte al giorno, con posologia aumentata la sera per permettere una efficace alcalinizzazione nottetempo.
Il citrato di K è segnalato come terapia nei PDTA (Percorsi Diagnostici, Terapeutici e Assistenziali) della Regione Lombardia e dunque anche se è un integratore, essendo prescritto nel piano terapeutico delle Malattie Rare, è completamente rimborsato dal SSN.
Nel prosieguo del follow-up, per nuove recidive, abbiamo prescritto a Luca un farmaco chelante la cistina, la tiopronina, che produce complessi tiopronina-cisteina che sono 50 volte più solubili della cistina. Dopo due mesi di terapia, compaiono eventi avversi (orticaria, dolori articolari, proteinuria). Un ulteriore tentativo terapeutico è stato avviato dopo tre anni con consenso informato del paziente e parere favorevole dell’allergologo, per la possibilità descritta di riprendere il trattamento dei chelanti senza eventi avversi dopo risoluzione della proteinuria. Purtroppo dopo poche settimane Luca manifesta incremento ponderale di 6 kg con dispnea ed edemi diffusi da stato anasarcatico per sindrome nefrosica con proteinuria massiva di 19 g/24h, che ha necessitato terapia con furosemide ed albumina ev. L’evoluzione è stata prognosticamente favorevole a breve, con scomparsa completa della proteinuria (7).
Secondo e terzo ostacolo nel percorso di cura: evento avverso alla tiopronina con reazione immunoallergica e sindrome nefrosica
Un nuovo approccio alternativo per la prevenzione delle recidive calcolotiche nella cistinuria si basa sulla inibizione della crescita dei cristalli con un L-cistina dimetil-estere e metil-estere in un modello murino di cistinuria, sia in vitro che in vivo. Purtroppo tali molecole sono instabili e possono portare ad un accumulo lisosomiale tossico di cistina, come nella cistinosi.
Nella ricerca ulteriore di prodotti efficaci, sono stati testati in un modello di topo Slc3a1-/- vari antiossidanti e il più promettente è risultato l’acido α-lipoico (ALA), grazie ad una azione inibitoria sulla crescita dei calcoli con effetto ancora inspiegato sulla incrementata solubilità della cistina. La buona notizia è che ALA è un integratore nutrizionale comunemente utilizzato nella neuropatia diabetica con profilo di rischio soddisfacente. Con tali presupposti, ALA è stato recentemente testato in due soggetti in età pediatrica con calcolosi cistinica che hanno manifestato ridotta incidenza di calcoli sintomatici e asintomatici e in un caso dissoluzione di alcuni calcoli fino a 9 mm dopo soli due mesi di terapia (8).
Decidiamo con Luca di iniziare la terapia con l’acido α-lipoico, sempre in associazione agli altri presidi noti di elevata diuresi alcalina che hanno comunque dato dei risultati tangibili nell’ultimo periodo almeno in una minore morbilità urologica. Dopo qualche settimana compare un’ingravescente perdita del gusto, non associato ad altra sintomatologia, che porta peraltro al dubbio di un’infezione da SARS-CoV-2 con immediata esecuzione di un tampone faringeo molecolare, risultato negativo. Tale sintomatologia non viene descritta come evento avverso in nessuna banca dati consultata, ma è senz’altro presente una causalità temporale con l’assunzione del nuovo farmaco. Purtroppo il fenomeno diventa incompatibile con l’alimentazione quotidiana e anche questa chance terapeutica viene preclusa.
Quarto ostacolo nel percorso di cura: evento avverso non noto all’acido α-lipoico con ageusia
ll racconto del percorso ad ostacoli della diagnosi e cura della calcolosi secondaria a cistinuria di Luca termina dopo più di 12 anni con una ulteriore delusione. Dovrà forzatamente affidarsi come strategia terapeutica al mantenimento costante di una efficace diuresi alcalina.
Siamo peraltro entrambi consapevoli e speranzosi in un futuro avanzamento delle ricerche farmacologiche per questa rara e “challenging” calcolosi renale (9).
Raccomandazioni per la pratica clinica
Memento: “Cistinuria, se non la cerchi, non la trovi”. Il dubbio diagnostico deve sorgere nell’evenienza di calcolosi insorta in età infantile, che deve sempre prevedere il dosaggio dei dibasico aminoacidi urinari e l’analisi spettrofotometrica o cristallografica di calcoli prodotti, ma può essere pure sospettata in pazienti adulti, dove la diagnosi di qualsivoglia tipo di calcolosi deve sempre essere formulata per un corretto inquadramento clinico.
A diagnosi fatta e terapia prescritta, l’iter successivo necessita una stringente valutazione della compliance e del puntuale raggiungimento e mantenimento dei goal terapeutici (diuresi quotidiana >3-4 L con pH urinario >7,5, oltre ad una eventuale corretta posologia dei farmaci chelanti) con controlli ambulatoriali e strumentali frequenti e ripetute prescrizioni per un trattamento che deve necessariamente durare tutta la vita.
In questo ambito, come in tutte le malattie rare, l’alleanza medico-paziente riveste un’importanza peculiare dai risultati a volte insperati.
Bibliografia
- Lieske JC, Rule AD, Krambeck AE, et al. Stone composition as a function of age and sex. Clin J Am Soc Nephrol. 2014;9:2141-2146.
- Eggerman T, Venghaus A, Zerres K. Cystinuria: An inborn cause of urolithiasis. Orphanet J Rare Dis. 2012;7:19.
- Sahota A, Tischfield JA, Goldfarb DS, et al. Cystinuria: Genetic aspect, mouse models, and a new approach to therapy. Urolithiasis. 2019;47:57-66.
- Dello Strologo L, Pras E, Pontesilli C, et al. Comparison between SLC3A1 and SLC7A9 cystinuria patients and carriers: a need for new classification. J Am Soc Nephrol. 2002;13:2547-2553.
- Rhodes HL, Yarram-Smith L, Rice SJ, et al. Clinical and genetic analysis of patients with cystinuria in the United Kingdom. Clin J Am Soc Nehrol. 2015;10:1235-1245.
- Servais A, Thomas K, Dello Strogolo L, et al. Cystinuria: Clinical practice recommendation. Kidney Int. 2020;99:48-58.
- Prot-Bertoye C, Lebbah S, Daudon M, et al. French Cystinuria Group. Adverse events associated with currently used medical treatments for cystinuria and treatment goals: results from a series of 442 patients in France. BJU Int. 2019;124:849-861.
- Cil O, Perwad F.α-lipoic acid (ALA) improves cystine solubility in cystinuria: report of 2 cases. Pediatrics. 2020;145:e20192951
- Moussa M, Papatsoris AG, Chakra MA, et al. Update on cystine stones: current and future concepts in treatment. Intractable & Rare Diseases Research. 2020;9:71-78.





